2026 Автор: Howard Calhoun | calhoun@techconfronts.com. Соңғы өзгертілген: 2025-06-01 07:14:24
Электрлік диссоциация біздің өмірімізде үлкен рөл атқарады, дегенмен біз әдетте бұл туралы ойламаймыз. Дәл осы құбылыспен сұйық ортадағы тұздардың, қышқылдардың және негіздердің электр өткізгіштігі байланысты. Сексен пайыз сұйық күйде болатын адам ағзасындағы «тірі» электр тогының әсерінен пайда болған алғашқы жүрек соғуларынан бастап, батареялары негізінен электрохимиялық батареялар болып табылатын автомобильдерге, ұялы телефондарға және ойыншыларға дейін электр диссоциациясы біздің маңайымызда көрінбейтін түрде болады.
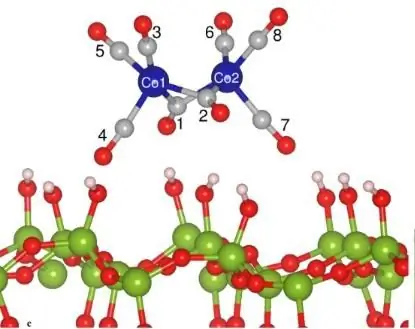
Жоғары температурада балқытылған бокситтен улы түтін шығаратын алып құмыраларда «қанатты» метал - алюминий электролиз арқылы алынады. Айналамыздағы бәрі, хром радиатор торларынан бастап, құлағымызда күміс жалатылған сырғаларға дейін, бір ретнемесе ерітінділермен немесе балқытылған тұздармен, демек, бұл құбылыспен кездеседі. Электрлік диссоциацияны ғылымның тұтас бір саласы - электрохимия зерттейтіні бекер емес.
Еріткен кезде еріткіш сұйықтың молекулалары еріген заттың молекулаларымен химиялық байланысқа түсіп, солваттар түзеді. Судағы ерітіндіде тұздар, қышқылдар және негіздер диссоциацияға ең сезімтал. Бұл процестің нәтижесінде еріген заттың молекулалары иондарға ыдырауы мүмкін. Мысалы, сулы еріткіштің әсерінен NaCl иондық кристалындағы Na+ және CI- иондары еріткіш ортаға өтеді. ерітілген (гидратталған) бөлшектердің жаңа сапасы.
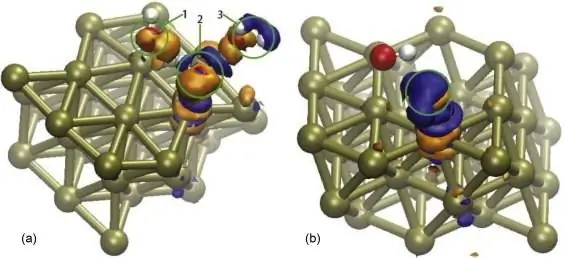
Еріткіш әсерінің нәтижесінде еріген заттың толық немесе ішінара иондарға ыдырау процесі болып табылатын бұл құбылыс «электрлік диссоциация» деп аталады. Бұл процесс электрохимия үшін өте маңызды. Күрделі көпкомпонентті жүйелердің диссоциациялануының сатылы ағынмен сипатталуының үлкен маңызы бар. Бұл құбылыспен ерітіндідегі иондар санының да күрт өсуі байқалады, бұл электролиттік заттарды электролиттік емес заттардан ажыратады.
Электролиз процесінде иондардың қозғалыс бағыты анық болады: оң зарядты бөлшектер (катиондар) - катод деп аталатын теріс зарядталған электродқа, ал оң иондар (аниондар) - анодқа, қарама-қарсы зарядты электрод, онда олар разрядталады. Катиондар тотықсызданады, ал аниондар тотығады. Демек, диссоциация қайтымды процесс.
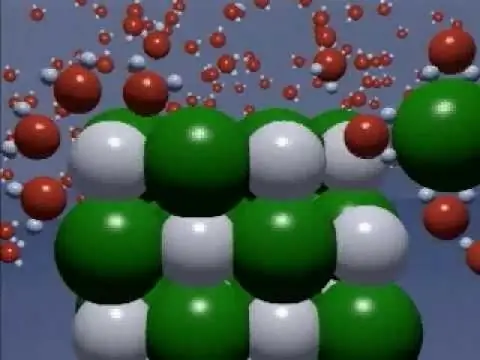
Бұл электрохимиялық процестің негізгі сипаттамаларының бірі гидратталған бөлшектер санының еріген зат молекулаларының жалпы санына қатынасы ретінде өрнектелетін электролиттік диссоциация дәрежесі болып табылады. Бұл көрсеткіш неғұрлым жоғары болса, электролит бұл зат соғұрлым күшті болады. Осы негізде барлық заттар әлсіз, орташа күшті және күшті электролиттер болып бөлінеді.
Диссоциациялану дәрежесі келесі факторларға байланысты: а) еріген заттың табиғаты; б) еріткіштің табиғатын, оның диэлектрлік өтімділігін және полярлығын; в) ерітіндінің концентрациясы (бұл көрсеткіш неғұрлым төмен болса, диссоциациялану дәрежесі соғұрлым жоғары болады); г) еріткіш ортаның температурасы. Мысалы, сірке қышқылының диссоциациясын келесі формуламен өрнектеуге болады:
CH3COOH H+ + CH3COO-
Күшті электролиттер қайтымсыз дерлік диссоциацияланады, өйткені олардың судағы ерітіндісінде бастапқы молекулалар мен гидратацияланбаған иондар болмайды. Сондай-ақ, химиялық байланыстың иондық және коваленттік полярлық түріне ие барлық заттар диссоциациялану процесіне ұшырайтынын қосу керек. Электролиттік диссоциация теориясын 1887 жылы көрнекті швед физигі және химигі Сванте Аррениус тұжырымдаған.
Ұсынылған:
Электрлік қаптау цехы: сипаттамасы, жабдықтары, қауіпсіздік талаптары, зияндылығы

Гапқыш цехы кез келген өндірісте өте маңызды сала болып табылады, дегенмен ол жоғары қауіптілігімен және зияндылығымен ерекшеленеді. Мұндай шеберханаларда жақсы желдету, өрт қауіпсіздігі және басқа да көптеген қорғаныс факторларын жабдықтау қажет
Электропластика. Электрлік қаптау технологиясы. Электрлік қаптау

Электролиз әдісімен бір металды екіншісімен қаптау әдісі. Бұл процедура дәстүрлі батыру әдістерін қолдану арқылы жүзеге асырылады
Электрлік балға: үлгілерге шолу

Бүгінгі күні мамандардың көмегінсіз үйде жөндеу жұмыстарын өз бетіңізше жүргізуге болады. Нарықта ұсынылған құрал тіпті күрделі орнату операцияларын қауіпсіз және қиындықсыз орындауға мүмкіндік береді. Бұл электр балғасының сипаттамаларымен расталады, соның арқасында көптеген адамдар тіпті қайта құруды жүзеге асырады. Сәйкес модельді таңдау ғана қалады
Қаржы-шаруашылық қызметін талдау – теориялық негіздері

Нарықтық қатынастарға көшу барлық кәсіпорындардан өндіріс тиімділігін арттыруды талап етеді, бұл өз кезегінде өнімінің бәсекеге қабілеттілігін арттырады. Бұл мәселені шешуде қаржылық-шаруашылық қызметті талдау ең маңызды рөл атқарады. Осы ғылыми пәннің көмегімен стратегиялық даму жоспарлары жасалып, басқару шешімдері ғылыми негізделеді, олардың орындалуы бақыланады
Электрлік көтергіш дегеніміз не? Жүктерді тік көтеруге арналған электрлік көтергіш

Мақала электрлік көтергішке арналған. Көтергіш қондырғының конструкциясы, оның пайдалану мүмкіндіктері мен сорттары қарастырылады

